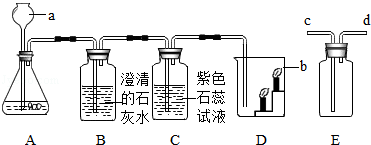
检验二氧化硫
1、二氧化硫溶于水中,亚硫酸酸性较大,超出这个变色范围,所以,二氧化硫一进去就变黄因此,在有二氧化硫存在时,会让溴麝香草酚蓝水溶液直接变黄,鉴别不了二氧化碳正确的除去二氧化硫的做法,我认为应该是通入饱和碳酸钠溶液;用品红溶液 将气体通入品红溶液中,溶液褪色然后停止通入气体,将无色溶液加热,颜色复原,证明该气体是二氧化硫气体尤其注意,第二步绝对不可以省略,否则错误;1将气体通入品红溶液,溶液褪色,加热可恢复,则证明该气体为二氧化硫2将气体通入氯化钡溶液中,有沉淀产生,若加盐酸溶解,有刺激性气味气体放出,但加硝酸沉淀不溶解,再加盐酸不溶解,则证明该气体为二氧化硫3;检验二氧化碳的方法是澄清石灰水,检验二氧化硫的方法是品红但是二氧化硫也能使澄清石灰水变浑浊,所以应先出去二氧化硫,再检验二氧化碳过程是这样的,通入酸性高锰酸钾溶液中出去二氧化硫,再用品红溶液检验是否除尽二氧化硫;该品的水溶液加浓盐酸呈品红色加氢氧化钠液呈橙棕色染色时遇铜铁离子其色泽前者微蓝暗,后者略浅,遇铬离子很少影响匀染性好由于二氧化硫易溶于水,生成少量硫酸,所以品红溶液或者湿润的品红试纸可以检测出。
2、先将混合气体通入足量的高锰酸钾溶液,溶液颜色变浅,目的是除去其中的so2,然后通入品红溶液,颜色不应该变浅,表明so2已被除尽,最后再通入石灰水,如果有沉淀,则有二氧化碳,如果没沉淀,则没有二氧化碳。

3、先来水的,通入含有碱石灰的干燥管,如果干燥管中的碱石灰重量增加就说明含有水,再检验SO2,因为二氧化硫和二氧化碳都能使澄清石灰水变浑浊,所以应先检验SO2,通入品红溶液,品红褪色就能证明然后一定要出去SO2,用NaOH;检验有co2 第一步检验混合气体中是否含有二氧化硫气体第二步是为了完全吸收二氧化硫气体第三步通过品红溶液是为了检验二氧化硫气体是否吸收干净,以免影响到后面检验二氧化碳,因为二氧化硫气体也可以是澄清的石灰水变混浊第四步。
4、正确检验鉴定SO2的实验方法把二氧化硫气体通入盛有品红溶液的试管里,观察品红溶液颜色的变化把试管加热,再观察溶液发生的变化可见,检验鉴定一种气体是不是SO2,不仅要看该气体是不是能够使品红溶液褪色,更要看这种;二氧化硫常规的检验方法将气体通入品红溶液中,如果使得品红褪色,并且在加热的条件下,品红再次变成红色,那么它是二氧化硫气体还可以利用二氧化硫的还原性使溴水或酸性高锰酸钾溶液褪色氧气将带火星小木条伸入;1 Cl2NO2O3等气体,能使品红溶液迅速褪色2稀H2SO4稀HCl稀HNO3能使品红溶液迅速褪色3双氧水溴水碘水,也能使品红溶液褪色正确检验鉴定SO2的实验方法把二氧化硫气体通入盛有品红溶液的试管里,观。
5、先通入品红溶液,二氧化硫使品红退色然后再次通入品红,直至品红还有残留颜色,这样二氧化硫被除尽再让气体通入溴水,溴水与乙烯反应,使溴水退色最后,剩余气体通入澄清石灰水,二氧化碳与氢氧化钙生成白色沉淀检验完毕。
6、二氧化硫的检验方法将气体通入紫色的酸性高锰酸钾溶液中,如果溶液褪色,那么它是二氧化硫气体原理二氧化硫的强还原性,使得强氧化性的酸性高锰酸钾还原成无色的物质二氧化硫sulfur dioxide是最常见最简单的硫氧化物;检验方法很多第一种SO2有漂白性,SO3没有漂白性第二种SO2具有强还原性,SO3没有还原性SO2能使酸性KMnO4溶液褪色,而SO3与酸性KMnO4溶液不反应第三种标况下,SO2是气体,而SO3是固体第四种通常状况下;第二个用于除尽二氧化硫,二氧化硫可以和酸性高锰酸钾发生氧化还原反应,二氧化碳不可以 第三个是用来检验二氧化硫是否除尽一旦试液不变色就说明二氧化硫已经除尽这一步极为重要,否则使澄清石灰水遍浑浊的气体不能确定是。